Des ingénieurs du MIT ont mis au point des tendons artificiels en hydrogel qui, connectés à du tissu musculaire vivant, augmentent drastiquement la force et la vitesse des robots biohybrides.
Cette avancée promet de rendre ces machines plus modulaires et efficaces, ouvrant la voie à des applications concrètes en micro-chirurgie ou en exploration de milieux hostiles.
La robotique biohybride, qui associe des tissus vivants à des composants synthétiques, représente une frontière fascinante de l'ingénierie. Depuis une décennie, des chercheurs conçoivent des robots capables de ramper, nager ou saisir des objets en utilisant de véritables muscles cultivés en laboratoire comme actionneurs.
Cependant, ces créations se heurtaient jusqu'à présent à des limites importantes en termes de puissance, de vitesse et de durabilité, principalement à cause de la connexion délicate entre le muscle mou et le squelette rigide.
Le tendon artificiel : un pont entre le vivant et le synthétique
Pour surmonter cet obstacle, une équipe menée par Ritu Raman au MIT a eu l'idée de s'inspirer de la nature en développant des tendons artificiels. Fabriqués à partir d'un hydrogel à la fois résistant et flexible, ces tendons agissent comme des connecteurs modulaires.
Ils ont été fixés de part et d'autre d'un petit morceau de muscle de laboratoire pour former une « unité muscle-tendon », puis reliés aux doigts d'une pince robotique. Cette innovation pourrait bien redéfinir les limites de la robotique miniature.
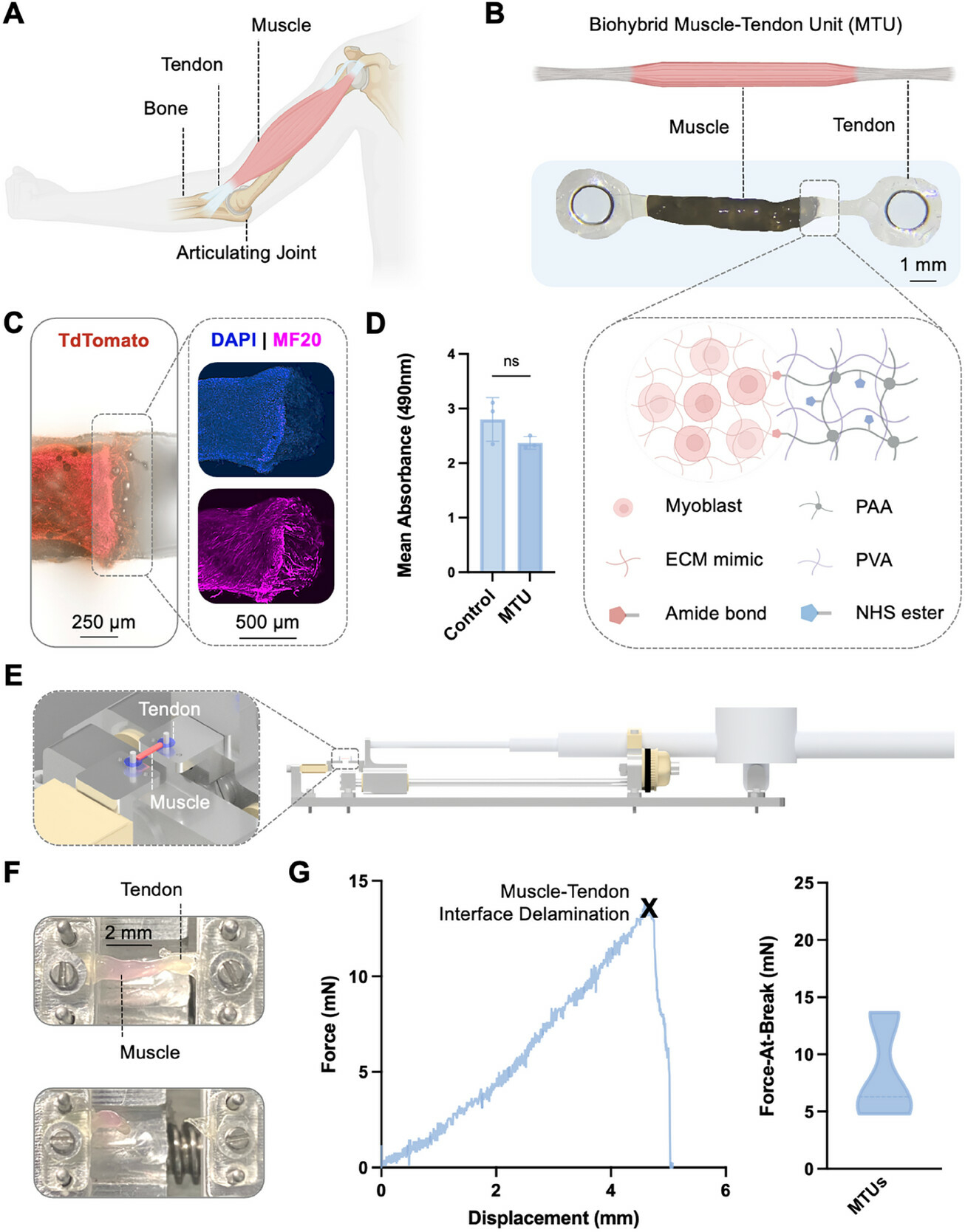
Les résultats de l'expérimentation sont sans appel. Lorsque le muscle central était stimulé pour se contracter, les tendons transmettaient la force à la pince avec une efficacité redoutable.
Le robot a pincé ses doigts trois fois plus vite et avec une force 30 fois supérieure par rapport au même design sans les tendons de connexion. De plus, le système a prouvé sa robustesse en maintenant cette performance sur plus de 7 000 cycles de contraction, démontrant une fiabilité remarquable.
Pourquoi le muscle est-il un actionneur d'avenir ?
L'intérêt pour les muscles en tant qu'actionneurs naturels ne cesse de croître. Contrairement aux moteurs traditionnels, qui deviennent difficiles à miniaturiser, chaque cellule musculaire est un actionneur indépendant capable de générer force et mouvement.
Loin des approches purement mécaniques vues chez des géants comme Tesla avec ses projets humanoïdes, cette branche explore une voie radicalement différente, misant sur les propriétés uniques du vivant.
Principe de l'unité muscle-tendon (credit : Advanced Sciences)
Les avantages sont multiples : un tissu musculaire peut se renforcer avec l'exercice et, surtout, se réparer naturellement en cas de blessure. Ces caractéristiques en font un candidat idéal pour des robots autonomes destinés à explorer des environnements dangereux ou inaccessibles, où aucune maintenance humaine n'est possible.
Cette vision s'oppose à la production de masse d'appareils électroniques à la conception et au fonctionnement figés en misant sur une croissance et une adaptation organiques.
Modularité et applications : vers une nouvelle ère pour les bio-bots ?
L'un des apports majeurs de cette recherche est la modularité. « Nous introduisons les tendons artificiels comme des connecteurs interchangeables entre les actionneurs musculaires et les squelettes robotiques », explique Ritu Raman.
Cette approche permet de ne plus « gaspiller » de tissu musculaire pour l'attache et de concentrer toute son énergie sur le mouvement. Sa standardisation pourrait faciliter la conception d'une vaste gamme d'applications, allant d'outils chirurgicaux microscopiques à des machines d'exploration adaptatives.
Le ratio puissance/poids du robot a été multiplié par 11, ce qui signifie qu'il faut beaucoup moins de muscle pour accomplir la même tâche. L'équipe du MIT travaille désormais sur les prochaines étapes, comme le développement d'enveloppes protectrices semblables à de la peau, pour préparer ces robots à des applications réelles et les faire sortir du laboratoire.